C’est à la fois un concept, une stratégie et un objectif. « One Health » (une santé) s’est progressivement imposé en sciences du vivant, en médecine vétérinaire et en sciences biomédicales. Il domine à présent la communication d’organisations internationales de santé publique comme l’Organisation mondiale de la santé animale, la Food and Agriculture Organization (Organisation des Nations unies pour l’alimentation et l’agriculture), l’Organisation mondiale de la Santé et les Centers for Disease Control and Prevention (centres pour le contrôle et la prévention des maladies). Mais le concept « One Health » reste peu connu du grand public et rarement intégré dans les prises de décision des gouvernements. Alors même que, représentant un véritable changement de paradigme, il pourrait nous aider à mieux appréhender, anticiper et gérer l’irruption de nouvelles pandémies.
L’évidente interconnexion du vivant
Le terme « one medicine » (une médecine) fut introduit en 1984 par Calvin Schwabe. L’épidémiologiste américain entendait alors souligner l’évidente interconnexion entre médecine animale et humaine. Mais il pointait également l’impérieuse nécessité d’une collaboration entre vétérinaires et médecins pour contrôler la dissémination des agents infectieux.
Sur les 1 407 agents pathogènes affectant l’humain, 58 % sont en effet d’origine animale, dont un quart capable d’une transmission potentiellement source d’épidémie ou de pandémie, à l’instar des virus Influenza et Ebola. De plus, 75 % des maladies infectieuses émergentes sont d’origine animale. Une meilleure compréhension et gestion des réservoirs animaux d’agents infectieux, mais aussi de leurs voies de transmission et d’adaptation à l’humain, s’avère donc indispensable au contrôle des zoonoses et des épidémies futures. D’où l’intérêt croissant pour l’éco-épidémiologie, discipline émergente et transversale à l’écologie, à l’épidémiologie et aux sciences biomédicales.
Ce sont des perturbations de la dynamique des interactions entre les populations d’humains, d’agents infectieux, de réservoirs animaux, et parfois d’insectes vecteurs, qui déclenchent en général les épidémies d’origine zoonotique. En faisant varier leur habitat ou leur abondance, des changements environnementaux, climatiques et socio-économiques peuvent par exemple modifier les probabilités d’interactions entre chaque population. Par ailleurs, les agents infectieux, et en particulier les virus à ARN, évoluent très rapidement. Ils peuvent donc s’adapter à de nouveaux hôtes s’ils entrent fréquemment en contact avec eux, créant ainsi un nouveau réseau d’interactions.
Chasse, déforestation, climat… et épidémies
Le lien entre l’intrusion de l’humain dans un écosystème et l’apparition d’une épidémie est bien illustré par le cas du virus de l’immunodéficience humaine (VIH), qui a fait plus de 32 millions de morts entre 1981 et 2018. Son émergence est vraisemblablement due à une augmentation de la chasse et de la consommation de viande de chimpanzé dans la région de Kinshasa (République démocratique du Congo) dans les années 1920-50 : les contacts alors accrus entre humains et primates infectés par le virus de l’immunodéficience simienne ont favorisé l’adaptation de cet agent pathogène à l’humain.
On peut également citer pour exemple la maladie de Lyme. Cette pathologie, qui témoigne des liens entre altération de la biodiversité et épidémies, est due à une bactérie, Borrelia burgdorferi, transmise par la morsure de tiques. Dans la nature, les tiques se nourrissent sur un grand nombre de vertébrés. Certains, comme les écureuils et les cervidés, sont assez résistants à l’infection. D’autres, telles les souris, y sont en revanche très susceptibles.
Suite à un effet de dilution, on trouve ainsi peu de tiques infectées dans les forêts présentant une grande biodiversité. Mais là où elle est faible, dans de petites parcelles boisées où les prédateurs sont donc peu nombreux, les souris peuvent voir leur nombre augmenter, ce qui accroît la fréquence d’infection des tiques et le risque pour l’humain : dans le nord-est des États-Unis et en Europe, un cycle historique de déforestation, de reboisement et de fragmentation des zones boisées a ainsi favorisé la progression de la maladie.
Dernier exemple emblématique : le réchauffement climatique. Il est désormais bien établi qu’il change la donne pour un large éventail de maladies à transmission vectorielle en Europe, et continuera de le faire dans les décennies à venir. On sait par exemple que le moustique tigre d’origine asiatique (Aedes albopictus), vecteur de maladies telles que Zika, la dengue et le chikungunya, ou encore la mouche des sables (phlébotome), originaire du Bassin méditerranéen et de l’Afrique du Nord et qui transmet la leishmaniose, se sont désormais établis dans le sud de l’Europe.
Une gestion tributaire du contexte sociétal
Pour gérer au mieux une épidémie, il importe de prendre en considération les réalités socio-économiques, politiques, religieuses et culturelles du pays concerné. Et l’adhésion des populations aux stratégies de santé publique est également indispensable. En somme, les stratégies de communication et d’éducation doivent s’adapter à chaque contexte sociétal.
Prenons le cas de la brucellose. Cette maladie est due aux bactéries Brucella, dont plusieurs espèces infectent de manière chronique les ruminants domestiques. L’humain peut être infecté par contact direct avec les animaux touchés ou, le plus souvent, suite à la consommation d’aliments contaminés, mais la transmission entre humains est quasi inexistante. Agir sur le réservoir animal permet ainsi de réduire les coûts économiques liés à la perte du bétail et d’améliorer la santé humaine.
En Europe, la brucellose a été quasiment éradiquée par la vaccination et l’abattage systématique des troupeaux infectés. Cette approche, toutefois, n’a été permise que par l’harmonisation des politiques sanitaires des différents pays – notamment l’identification des animaux domestiques, leur testage et le contrôle de leurs mouvements – et l’indemnisation des éleveurs. Or on ne peut pas l’appliquer aux pays en voie de développement, où les ressources économiques comme les capacités opérationnelles des services vétérinaires sont limitées. Prenons le cas de l’Inde, où la brucellose reste endémique. Le manque de compensation financière octroyée aux fermiers et l’interdiction d’abattage des bovins pour motifs religieux rendent impossibles le testage et l’élimination des animaux infectés. C’est pourquoi, dans ce pays, seule une stratégie basée sur la vaccination s’avère viable.
Une approche multidimensionnelle et pluridisciplinaire
Les “12 principes de Manhattan” ont été présentés en 2004 à New York (États-Unis), lors d’une conférence organisée par la Société pour la conservation de la vie sauvage (Wildlife Conservation Society).
Le premier de ces principes insiste sur la nécessaire reconnaissance des liens entre santé humaine, santé animale et environnement. Mais est aussi pointée la nécessité d’approches holistiques et prospectives des maladies infectieuses émergentes tenant compte des interconnexions complexes entre espèces. Ou encore, celle d’une réduction du commerce d’animaux sauvages en raison de « la menace réelle qu’il représente pour la sécurité socioéconomique mondiale » ; d’une augmentation des investissements dans les infrastructures de santé et les réseaux de surveillance des maladies infectieuses ; d’un partage rapide et clair des informations ; d’une éducation et d’une sensibilisation des populations et des décideurs politiques à l’interconnexion du vivant.
La conclusion livrée dans le résumé du congrès est sans appel : « Résoudre les menaces d’aujourd’hui et les problèmes de demain ne peut être accompli avec les approches d’hier ». « Nous devons concevoir des solutions adaptatives, prospectives et multidisciplinaires aux défis qui nous attendent sans aucun doute. »
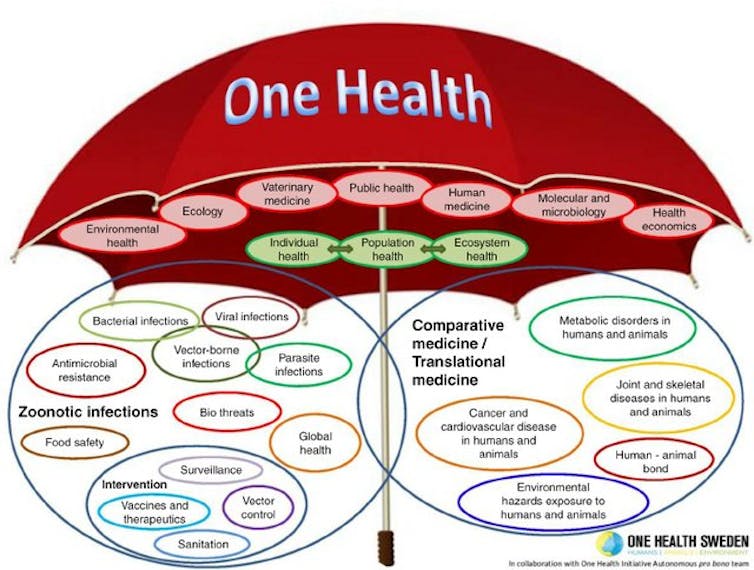
One Health Initiative
Le concept « One Health » fut introduit en 2008 à Sharm el-Sheikh (Égypte), lors d’un symposium sur les risques infectieux liés aux contacts des écosystèmes humain et animal. Peu après, suite à la pandémie de grippe A due au virus H1N1 de 2008-2009, l’OMS adoptait un programme mondial de lutte contre la grippe impliquant une surveillance accrue des réservoirs animaux. Et dans le même temps, une première agence One Health était créée aux États-Unis. Elle œuvre aujourd’hui à promouvoir un agenda mondial de la sécurité sanitaire, en coopération avec de nombreuses autres organisations nationales et internationales, et implique une soixantaine de pays.
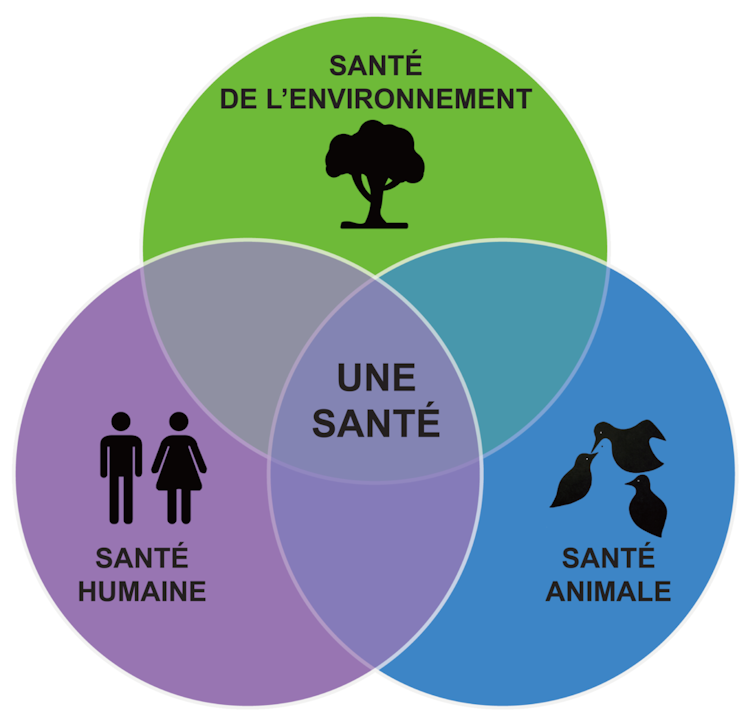
Wikipedia
Depuis l’émergence de « One Health », d’autres concepts s’en rapprochant plus ou moins ont vu le jour, comme EcoHealth et Planetary Health. Tenant compte de l’interconnexion du vivant, mais aussi du nécessaire abandon de toute réflexion linéaire et réductrice, et ayant en commun un décloisonnement des disciplines, ces nouveaux concepts devraient permettre de mieux appréhender et gérer les crises sanitaires.
De l’importance d’anticiper
Nous vivons tous dans le même monde, et notre santé comme notre économie dépendent étroitement de son état. Si nous voulons atteindre les objectifs du millénaire pour le développement durable des Nations unies, il faut impérativement tenir compte des multiples interactions entre santé publique, économie, santé animale et environnement. Force est néanmoins de constater que la vision « One Health » est rarement adoptée par les décideurs politiques, comme l’a mis en lumière la gestion chaotique de la pandémie de Covid-19.
Alors que l’émergence de nouvelles pandémies virales d’origine zoonotique avait été maintes fois prédite par la communauté scientifique, les gouvernements se sont montrés incapables d’anticiper. Pire : ils ont mis en place des mesures nationales hétéroclites (et parfois contradictoires), alors qu’une pandémie est à l’évidence un problème global nécessitant une action concertée supranationale.
Bien entendu, nous devons en tirer des leçons. Dans la vision « One Health », la pandémie induite par le SARS-CoV-2 est la conséquence directe et prévisible de la mondialisation des systèmes de production animale, de la vente d’animaux sauvages vivants, mais aussi du tourisme de masse, du commerce international et de l’hypermobilité qui les accompagne. Et nonobstant ce que d’aucuns sous-entendent, on ne peut pas l’interpréter comme un cygne noir, un événement inopiné qui a une cause externe à notre système économique libéral.![]()
Eric Muraille, Biologiste, Immunologiste. Maître de recherches au FNRS, Université Libre de Bruxelles et Jacques Godfroid, Professor of Microbiology, University of Tromsø
Cet article est republié à partir de The Conversation sous licence Creative Commons. Lire l’article original.
